Seit mehr als 30 Jahren
Bioverfügbarkeit von Zink
Vergleich der Bioverfügbarkeit von Zink aus drei unterschiedlichen Präparaten in vitro.
Angefertigt durch die BIOTESYS GmbH (2007-August)
Im Rahmen dieses Projekts wurde die Bioverfügbarkeit von Zink aus drei unterschiedlichen Präparaten in Darmzellen (CaCo-2) in vitro untersucht.
Einführung
Zum Vergleich der Aufnahme von Zink aus den drei unterschiedlichen Präparaten wurde angenommen, dass alle Präparatformen nach der oralen Aufnahme und der Passage des Magens in flüssiger Suspension vorliegen. Die Aufnahme von Zink aus der Nahrung erfolgt im Dünndarm. Für in vitro Versuche geeignete Modelle auf Basis von Dünndarmzellen existieren nicht, daher wurde auf Zellen zurückgegriffen, welche als die im Moment beste Darmmodelzelllinie gelten – CaCo-2. Diese Zellen wurden auf Zellkulturinserts kultiviert. Es war dadurch möglich, ein polares Epithelmodell zu simulieren. Auf einer Seite der Zellschicht erfolgte die Versorgung mit Nährmedium, während auf der anderen Seite die Testpräparate appliziert wurden. Die Aufnahme von Zink in die Zellen war dabei das Testkriterium. Um die Vergleichbarkeit zwischen den unterschiedlichen Formulierungen zu gewährleisten, wurden die Präparate so verdünnt, dass allen „Darmmodellen“ dieselbe Zinkkonzentration dargeboten wurde. Vor Beginn dieser Aufnahmeuntersuchungen wurde in Zytotoxassays geprüft, welche maximale Konzentration der Präparate die Zellen nicht schädigt.
Testmaterial
- Zink Reu-Rella® Presslinge – Haltbarkeit 12.6.2008; Charge 9516 (C/No.1-10)
- Unizink Tabletten Tabletten – Haltbarkeit 10.2010; Charge 05325
- Curazink Kapseln – Haltbarkeit 06.2009; Charge 5363
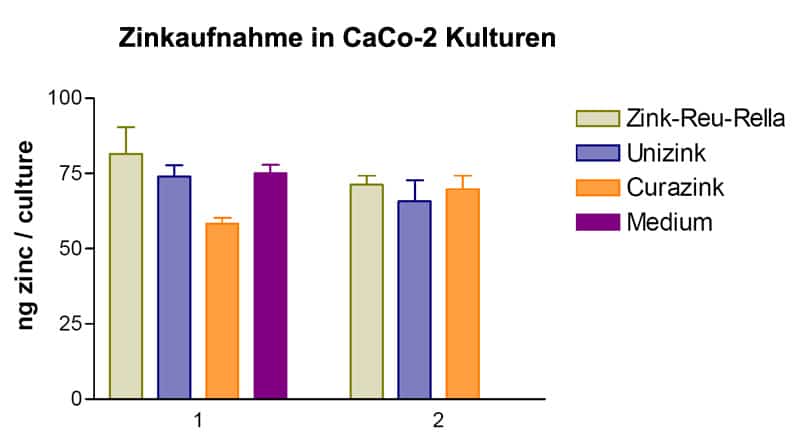
Prüfung der Zinkaufnahme in CaCo-2 Zellen. Dargestellt werden die Mittelwerte der beiden unabhängigen Durchgänge + SEM. Jeder Balken repräsentiert vier Messwerte. Supplementiert wurden (1.) 167,75 ng Zink / mL bzw. (2.) 83,75 ng Zink / mL.
Die Verdünnungsreihe ergab, dass Kulturen, welche mit Curazink in der Verdünnung 1:2 inkubiert wurden, absterben. Auch die Verdünnung 1:10 des Präparats Curazink führte noch zu einem Rückgang der lebenden Zellen auf ca. 20% der Kontrollkultur. Kulturen, welche mit Suspensionen der Zink-Reu-Rella® Tablette in der Verdünnung 1:2 bzw. 1:10 behandelt wurden, zeigen einen Rückgang der viablen Zellen auf 70-75% der Kontrolle. Alle anderen Kulturen zeigen keinen nennenswerten Rückgang der Viabilitäten. Auf Grund dieser Ergebnisse und unter Berücksichtigung der Zink-Gehalte der drei Präparate wurde die Verdünnung 1:100 von Zink-Reu-Rella® als Maßstab für die Supplementierung gewählt, die Verdünnungen der drei Präparate wurden jeweils auf 167,75 ng Zink / mL Supplementierungslösung eingestellt.
Aufnahme von Zink aus den eingestellten Verdünnungen
Die, wie oben dargestellt, kultivierten Modelle wurden nach 14-tägiger Kultur in den Aufnahmekinetiken eingesetzt. Es wurden zwei unabhängige Durchgänge mit je zwei gleichbehandelten Replikaten pro Durchgang durchgeführt. Darüber hinaus wurden zwei Verdünnungen der Präparatsuspensionen eingesetzt (1. 167,75 ng / mL und 2. 83,875 ng / mL).
1. Supplementierung mit 167,75 ng Zink / mL:
Die Ergebnisse zeigen einen leicht erhöhten Gehalt der Zellen an Zink nach Supplementierung mit der Zink-Reu-Rella®-Suspension. Die Supplementierung mit Suspensionen aus Unizink oder Curazink zeigte keinen erhöhten Zinkgehalt. Kulturen welche nur mit Medium (Kontrolle) supplementiert wurden, enthalten ebenfalls Zink, jedoch etwas weniger als Kulturen, welche mit Zink-Reu-Rella® supplementiert wurden. Mit Unizink supplementierte Kulturen weisen den gleichen Zinkgehalt auf wie die nur mit Medium behandelten. Hier wurde also kein zusätzliches Zink aufgenommen. Auffallend ist der reduzierte Gehalt nach Behandlung mit Curazink. Dies könnte auf einen Auswascheffekt des Präparates zurückzuführen sein. Die Unterschiede zw. den Zinkgehalten der Gruppen sind bis auf die Gruppen Zink-Reu-Rella® und Curazink nicht siginifikant (p= < 0,05).
2. Supplementierung mit 83,875 ng Zink / mL:
Nach der Supplementierung mit der höheren Verdünnung der Testpräparate (halbierte Konzentration gegenüber der 1. Supplementierung) konnte keine Zinkaufnahme festgestellt werden. Die Zinkgehalte der Kulturen bleiben auf dem Niveau der Kontrollkulturen. Auch der Auswascheffekt bei Curazink ist nicht mehr zu beobachten, dies ist wahrscheinlich auf die weitere Verdünnung der Begleitstoffe im Präparat zurückzuführen. Die Rezeptur des Mediums weist kein Zink auf, daher kommt als einzige Quelle das foetale Rinderserum in Frage, welches dem Medium zugesetzt werden muss. Der Gehalt des Serums an Zink ist nicht bekannt, jedoch wurden alle Verdünnungen der Zinkpräparate mit demselben Medium und damit mit dem selben Serumanteil erstellt. Es ist also davon auszugehen, dass alle Kulturen über das Medium dieselbe Menge an Zink angeboten bekamen. Über die Präparate wurde zusätzliches Zink jedoch in allen Fällen in der gleichen Menge angeboten. Der Unterschied zw. den Supplementierungsgruppen besteht also nur in den Inhaltsstoffen der Präparate. Durch diesen Ansatz wird gewährleistet, dass sich der Vergleich nur auf die Formulierungen bezieht.
Die Vermessung der Waschpuffer, die vor der Ernte der Zellen gewonnen wurden, ergab Messwerte unterhalb der Bestimmungsgrenze der Analyse (< 10 ng/ mL). Damit ist der Nachweis erbracht, dass die Messwerte der Zellpellets auf intrazellulärem Zink beruhen und nicht auf an der Zelloberfläche haftenden Präparats.
Fazit
Unter den beschriebenen Versuchsanordnungen zeigt Zink Reu-Rella als einziges der Präparate einen über die Kontrolle hinausgehenden Zinkgehalt und daher die beste Aufnahmeeffektivität.
